Executive Summary
투자 테제: HLB는 간암 1차 치료제 리보세라닙+캄렐리주맙 병용요법이 FDA에 두 차례 거절당하면서 52주 고점 대비 46% 급락했다. 그러나 거절 사유는 약물의 효능이 아닌 제조시설(CMC) 문제였고, 이 병용요법은 mOS 23.8개월로 현존 간암 치료제 중 최장 생존기간을 기록하며 BCLC·ESMO 국제 가이드라인에 FDA 승인 전부터 등재되는 이례적 성과를 거뒀다. 시장은 "FDA 두 번 거절"이라는 공포에 갇혀 있다.
| 핵심 지표 | 수치 |
|---|---|
| 현재가 | 52,400원 (2026.02.11 기준) |
| 52주 고점 | 97,600원 |
| 52주 고점 대비 | -46.3% |
| 52주 저점 | 36,150원 |
| 시가총액 | ~7조원 (코스닥 9위) |
| FDA 간암 신약 재신청 | 2026.01.23 접수 완료 |
| FDA 심사 분류 | Class 2 (6개월 심사) |
| 간암 mOS (전체생존기간) | 23.8개월 (현존 최장) |
| FDA 담관암 신약 NDA | 2026.01.27 신청 완료 |
Re:Discovery 판단: FDA가 거절한 이유가 "약이 안 듣는다"가 아니라 "공장 문제"였다는 사실을 시장은 구분하지 않는다. 전 세계 암 전문의들이 이미 치료 가이드라인에 올려놓은 약이, 제조시설 보완이라는 마지막 관문 앞에 서 있다. 2026년 하반기가 HLB의 운명을 결정한다.
1. 왜 소외됐나: "FDA 두 번 거절"이라는 낙인
HLB의 추락은 반복된 실패의 트라우마가 만들어낸 것이다.
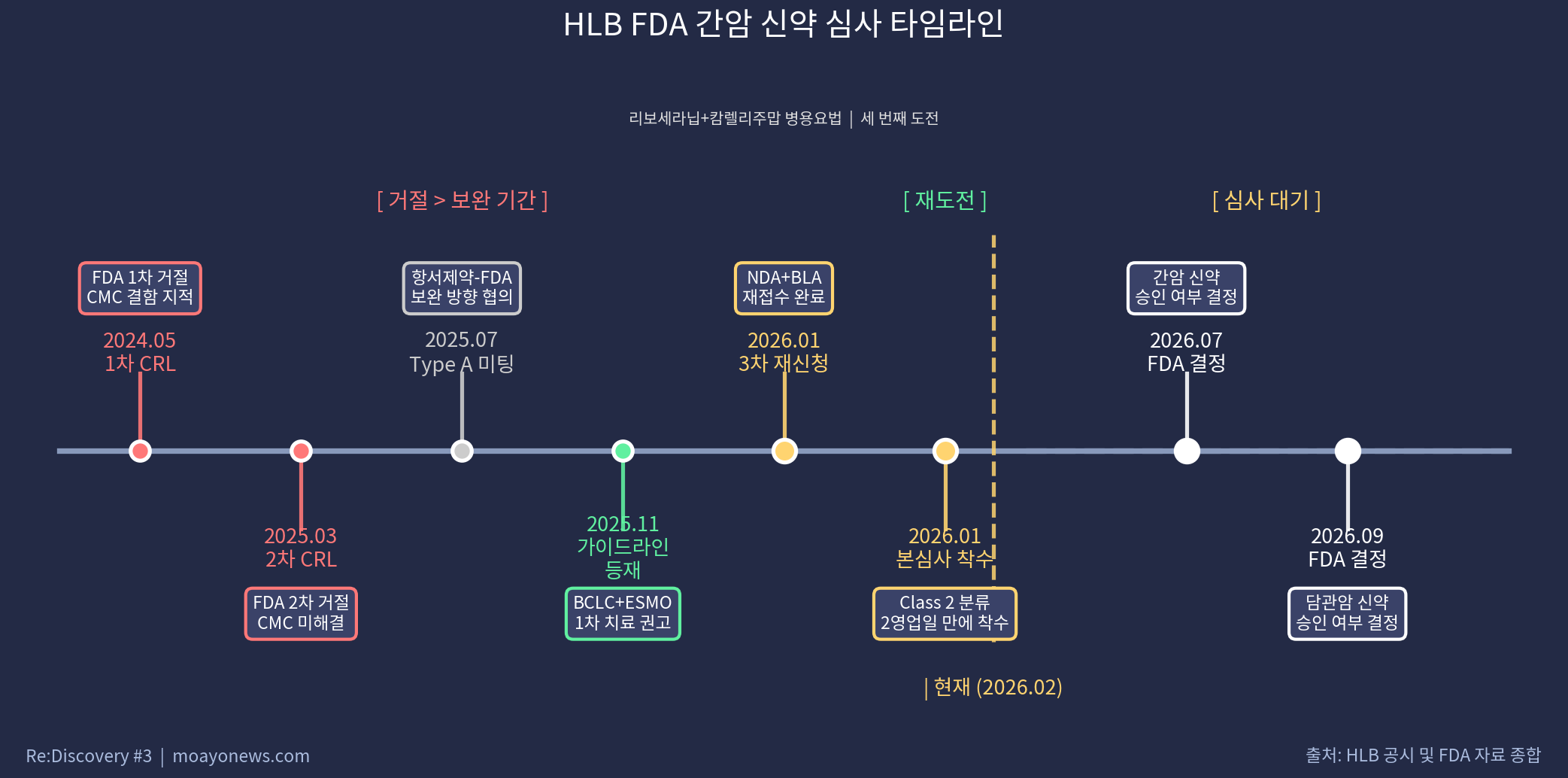
타임라인:
| 시점 | 주가 | 이벤트 |
|---|---|---|
| 2015 | - | 미국 엘레바 테라퓨틱스 인수, 신약 개발 진출 |
| 2023.07 | - | 임상 3상 결과 란셋(The Lancet) 게재 |
| 2024.05 | 급락 | FDA 1차 CRL (보완요청서) - 제조시설 결함 |
| 2025.03 | 급락 | FDA 2차 CRL - CMC 미해결 |
| 2025.03 | - | ESMO 가이드라인 간암 1차 치료 등재 |
| 2025.07 | - | 항서제약-FDA 타입 A 미팅, CMC 보완 착수 |
| 2025.11 | - | BCLC 가이드라인 간암 1차 치료 등재 |
| 2025.11 | - | 란셋 종양학(Lancet Oncology) 최종 분석 게재 |
| 2026.01.23 | 66,700원 | FDA 3차 재신청(NDA) 접수 |
| 2026.01.28 | - | FDA, 2영업일 만에 본심사 착수 승인 (Class 2) |
| 2026.02.11 | 52,400원 | 현재 (재신청 이후 오히려 하락) |
핵심 논점: 시장은 "FDA가 두 번이나 거절했다"는 사실만 기억한다. 그러나 CRL(보완요청서)의 내용을 뜯어보면 이야기가 완전히 달라진다. FDA는 리보세라닙 자체의 안전성이나 유효성에 대해 단 한 차례도 문제를 제기하지 않았다. 거절 사유는 파트너사 항서제약의 캄렐리주맙 생산 공장에서 발견된 CMC(화학·제조·품질관리) 결함이었다.
"약은 좋은데 공장이 문제" — 이것이 HLB 스토리의 본질이다.
2. 뭐가 바뀌었나: 전 세계가 먼저 인정한 약
FDA 승인도 받기 전에 국제 치료 가이드라인에 먼저 올라간 약. 이것이 리보세라닙의 현재 위치다.
글로벌 임상 3상 (CARES-310) 최종 결과
| 지표 | 리보+캄렐 | 소라페닙 (대조군) |
|---|---|---|
| 전체생존기간(mOS) | 23.8개월 | 15.2개월 |
| 객관적 반응률(ORR) | 27% | 6% |
| 반응지속기간(mDOR) | 17.5개월 | 9.2개월 |
| 12개월 생존율 | 77% | 61% |
| 24개월 생존율 | 49% | 33% |
| 36개월 생존율 | 38% | 25% |
| 위험비(HR) | 0.64 (통계적 유의) | |
| 치료중단 비율 | 3.7% | 5~43% (타 치료제) |
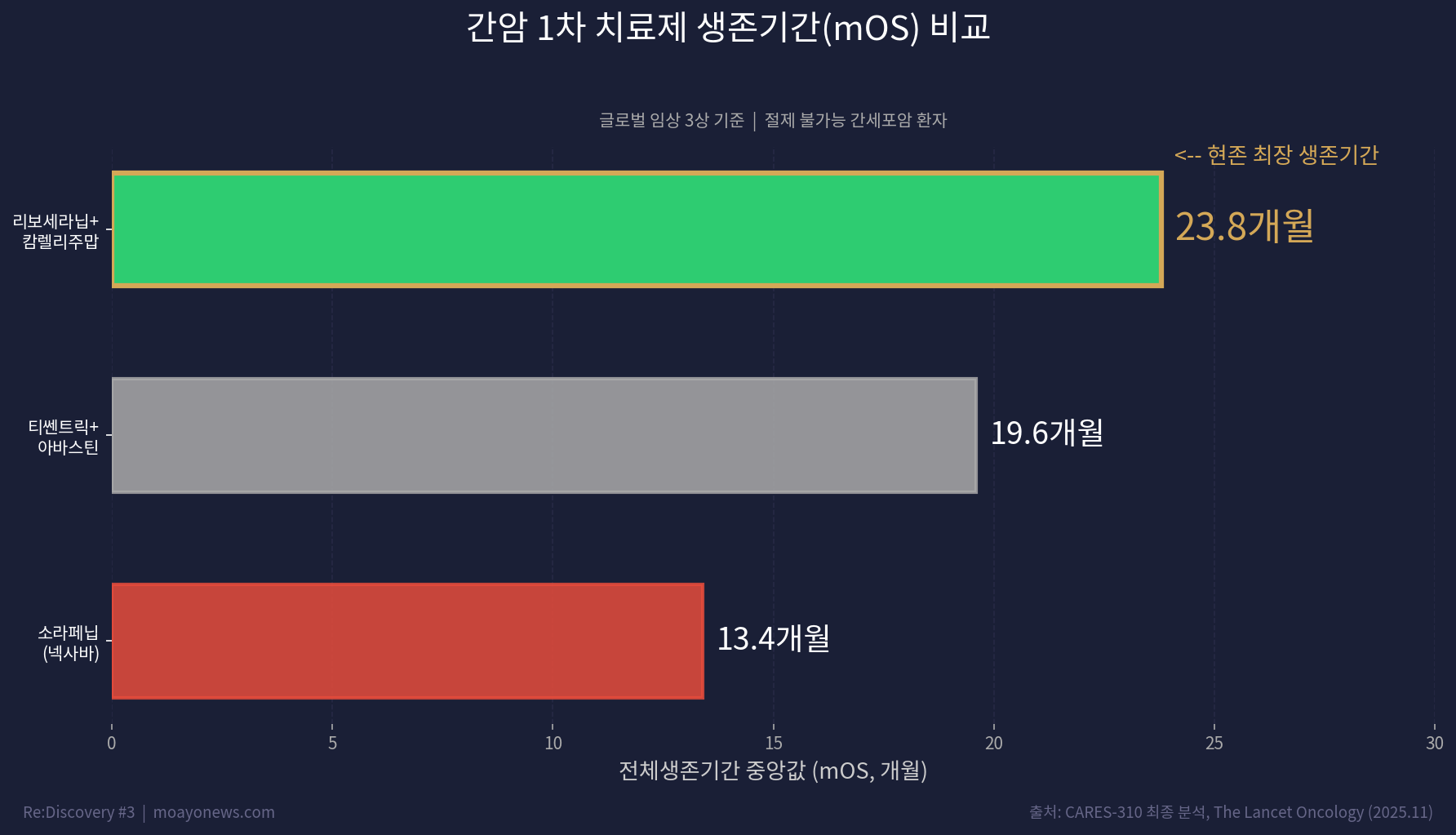
mOS 23.8개월의 의미: 간암은 "침묵의 장기"인 간에 발생해 말기에 발견되는 경우가 많다. 수술이 불가능한 진행성 간암 환자의 5년 생존율은 약 20%에 불과하다. 10년 넘게 표준 치료제였던 소라페닙(넥사바)의 mOS가 13.4개월, 현재 표준인 아테졸리주맙+베바시주맙(티쎈트릭+아바스틴)이 19.6개월인데, 리보+캄렐은 23.8개월이다. 간암 치료 역사상 가장 긴 생존기간.
3. 비즈니스 모델: 간암 1차 치료의 새 표준
작용 기전: 협공 전략
리보세라닙+캄렐리주맙 병용요법은 암세포를 두 방향에서 동시에 공격한다. 리보세라닙(VEGFR-2 억제제)은 암세포가 스스로 만드는 혈관을 차단해 영양 공급을 끊는다. 캄렐리주맙(PD-1 항체)은 면역세포의 브레이크를 해제해 암세포를 직접 공격하게 한다. 혈관 차단 + 면역 활성화의 이중 공격이 핵심이다.
간암 1차 치료제 비교:
| 치료제 | mOS | 유형 | 상태 |
|---|---|---|---|
| 리보세라닙+캄렐리주맙 | 23.8개월 | TKI+PD-1 | FDA 심사 중 |
| 티쎈트릭+아바스틴 | 19.6개월 | PD-L1+항VEGF | 현재 표준 |
| 소라페닙 (넥사바) | 13.4개월 | TKI 단독 | 과거 표준 |
| 렌바티닙+펨브롤리주맙 | - | TKI+PD-1 | 임상 실패 |
| 카보잔티닙+아테졸리주맙 | - | TKI+PD-L1 | 임상 실패 |
주목할 점은 TKI+면역항암제 조합으로 간암 1차 치료에서 유효성을 입증한 약이 리보+캄렐이 유일하다는 사실이다. 렌바티닙+키트루다, 카보잔티닙+아테졸리주맙 모두 실패했다. 그리고 리보+캄렐은 현재 표준인 티쎈트릭+아바스틴보다 4.2개월 더 긴 생존기간을 보여줬다.
추가 강점: 아바스틴 병용요법은 위장관 출혈 위험 때문에 치료 전 반드시 내시경을 해야 하지만, 리보+캄렐은 이 과정이 불필요해 더 빠르게 환자를 치료할 수 있다.
4. 파이프라인: 간암만이 아니다
HLB는 2026년 두 개의 FDA 신약 승인을 동시에 노리고 있다.
| 파이프라인 | 적응증 | 핵심 데이터 | 예상 승인 |
|---|---|---|---|
| 리보세라닙+캄렐리주맙 | 간암 1차 | mOS 23.8개월 | 2026년 7월 |
| 리라푸그라티닙 | 담관암 2차 | ORR 46.5% | 2026년 9월 |
리라푸그라티닙: 담관암의 게임체인저
HLB의 두 번째 신약은 FGFR2 융합·재배열 표적 항암제 리라푸그라티닙이다. 담관암 2차 치료제로 개발 중이며, 간암과는 별개의 심사 트랙으로 진행된다.
담관암 임상 2상 (ReFocus) 결과:
| 지표 | 리라푸그라티닙 | 페미가티닙 | 푸티바티닙 |
|---|---|---|---|
| 객관적 반응률(ORR) | 46.5% | 36% | 42% |
| 반응지속기간(mDOR) | 11.8개월 | 9.1개월 | 9.7개월 |
| 고인산혈증 발생률 | 20.7% | 60% | 85% |
| 치료중단 비율 | 4.3% | 9% | 4.9% |
리라푸그라티닙은 FDA로부터 희귀의약품(2022), 혁신신약(2023) 지정을 받았고, 임상 3상 없이 임상 2상만으로 가속승인 경로를 통한 NDA에 합의했다. 우선심사 지정 시 9월경 승인 여부 결정 전망.
5. 밸류에이션: FDA 승인 여부에 모든 것이 달려 있다
HLB는 전형적인 바이오 기업으로, 현재 실적만으로는 밸류에이션을 논하기 어렵다. 시가총액 약 7조원은 오직 신약 승인에 대한 기대를 반영한 것이다.
시나리오 분석:
| 시나리오 | 확률 | 임팩트 |
|---|---|---|
| 간암+담관암 모두 승인 | 낙관적 | K-바이오 역사적 이정표, 급등 예상 |
| 간암 승인 + 담관암 보류 | 기본 시나리오 | 상업화 원년 진입, 상승 예상 |
| 간암 3차 CRL | 리스크 | 신뢰 붕괴, 52주 저점(36,150원) 재시험 |
| 두 건 모두 실패 | 최악 | 기업 존립 위기 수준의 하락 |
HLB 투자의 핵심은 **"CMC 문제가 진짜 해결됐느냐"**에 대한 판단이다. 항서제약이 10개월간 제조 공정을 보완했고, FDA와 타입 A 미팅까지 거쳤으며, 재신청 2영업일 만에 본심사 착수가 승인됐다는 것은 긍정적 신호다.
6. 촉매: 6개월 안에 운명이 갈린다
| 촉매 | 시점 | 의미 |
|---|---|---|
| FDA 제조시설 실사 | 2026 상반기 | 항서제약 공장 실사 통과 여부가 최대 관건 |
| 간암 신약 FDA 결정 | 2026년 7월경 | Class 2 기준 6개월 심사 |
| 담관암 신약 본심사 착수 | 2026년 3~4월 | 우선심사 지정 여부 확인 |
| 담관암 신약 FDA 결정 | 2026년 9월경 | 가속승인 경로, 우선심사 시 |
| 중국 간암 TACE 병용 허가 심사 | 2026년 중 | 중국 시장 추가 적응증 확대 |
FDA 재신청 후 2영업일 만에 본심사 착수가 승인된 것은 이례적으로 빠른 속도다. 통상 1개월이 소요되는 절차가 48시간 만에 완료됐다는 것은, FDA가 이미 이 약의 유효성 데이터에 대해서는 충분히 검토를 마쳤다는 방증일 수 있다. 남은 것은 공장 실사뿐이다.
7. 리스크 요인
단기 리스크
- •3차 CRL 가능성: CMC 보완이 불충분할 경우 세 번째 거절도 가능하며, 이 경우 주가 충격은 이전보다 클 수 있음
- •항서제약 리스크: 중국 파트너사의 제조 품질에 HLB의 운명이 좌우되는 구조적 약점
- •수급 불안: 바이오 섹터 전반의 센티먼트 악화 시 동반 하락 위험
- •높은 변동성: FDA 관련 뉴스에 따라 일일 10% 이상 등락 가능
중장기 리스크
- •상업화 실행력: FDA 승인 후에도 미국 시장에서 영업·유통 인프라 구축이 필요
- •경쟁 심화: 간암 치료제 시장에 신규 진입자 증가 가능성
- •재무 부담: 지속적 영업적자 상태에서 상업화 비용까지 소요
- •미중 관계 리스크: 중국 항서제약과의 파트너십에 지정학적 리스크 내재
8. 차트분석: 기술적 관점
주요 기술적 레벨:
| 구분 | 가격 | 의미 |
|---|---|---|
| 52주 저점 | 36,150원 | 2차 CRL 직후 저점, 강한 지지선 |
| 단기 지지선 | 50,000원 | 심리적 지지선, 최근 거래 하단 |
| 현재가 | 52,400원 | 52주 범위 하위 26% |
| FDA 재신청일 종가 | 66,700원 | 1차 저항선, 재신청 기대감 반영 가격 |
| 중기 저항선 | 75,000~80,000원 | 승인 기대 선반영 구간 |
| 52주 고점 | 97,600원 | FDA 승인 확정 시 돌파 시도 구간 |
주목할 패턴은 FDA 재신청(1/26) 이후 주가가 66,700원에서 52,400원까지 21% 하락했다는 것이다. "소문에 사서 뉴스에 팔아라"의 전형이지만, 동시에 시장이 3차 승인에 대한 확신을 갖지 못하고 있다는 의미이기도 하다. 결국 실사 결과가 나올 때까지 박스권에 갇힐 가능성이 높다.
9. 결론: Re:Discovery 관점
HLB는 **"반복된 실패의 트라우마 vs 압도적 임상 데이터"**가 충돌하는 극적인 사례다.
| 시장이 기억하는 것 | 시장이 놓치고 있는 것 |
|---|---|
| FDA 두 번 거절 | 거절 사유는 약효가 아닌 공장 문제 |
| 바이오 불확실성 | BCLC·ESMO 가이드라인 FDA 승인 전 등재 |
| 재신청 후에도 주가 하락 | mOS 23.8개월, 간암 치료 역사상 최장 |
| 중국 파트너사 의존 | 항서제약 10개월 보완 + FDA 타입A 미팅 완료 |
| 간암 하나에 올인 | 담관암 2차 신약(리라푸그라티닙) 동시 FDA 심사 |
Re:Discovery 시각: HLB는 알테오젠이나 Upstart와는 성격이 다르다. 실적으로 증명된 기업이 아니라, 한 번의 승인 결정에 모든 것이 걸린 이벤트 드리븐 종목이다. 그러나 그 이벤트의 성공 확률을 냉정하게 따져보면, 시장이 반영한 것보다 높을 수 있다. 약의 효능은 최고, 거절 사유는 보완 가능한 영역, 전 세계 종양학회가 이미 인정, 재신청 후 2일 만에 본심사 착수. 2026년 7월, FDA의 세 번째 대답이 HLB의 10년 도전에 마침표를 찍게 된다.
본 리포트는 정보 제공 목적으로 작성되었으며, 특정 종목의 매수·매도를 권유하지 않습니다. 투자 판단과 그에 따른 책임은 투자자 본인에게 있습니다. 특히 바이오 주식은 FDA 승인 여부에 따라 극단적 변동성을 보일 수 있으므로 각별한 주의가 필요합니다.
📚 NDA(신약허가신청)란 무엇인가? — FDA에 신약 승인을 신청하는 절차, CRL(보완요청서)과의 관계, 심사 분류(Class 1·2)의 차이를 알아보세요.